Qu’est-ce que la lumière et d’où vient-elle ?

Photo par Nadine Shaabana sur Unsplash
Introduction – Qu’est-ce que la lumière ?
En tant que non-scientifiques, nous tenons pour acquis que la lumière n’est que de la lumière, et nous ne pensons guère à son origine ou à son mode de production. Si vous travaillez dans le domaine de la lumière, de l’éclairage ou même de l’agriculture d’intérieur, nous avons pensé que vous aimeriez en savoir plus.
Cet article lève le voile sur la question « Qu’est-ce que la lumière ?

Fig 1 Photo d’Umberto sur Unsplash
La lumière est une libération d’énergie.
En bref, les photons de lumière émis par une source lumineuse (par exemple une ampoule à incandescence) constituent simplement une libération d’énergie. Pour expliquer cela, prenons l’analogie d’un élastique qui claque.
Supposons que vous appliquiez une énergie physique pour séparer l’élastique. L’énergie est ainsi transmise au matériau de l’élastique sous forme d’énergie potentielle. Lorsque vous relâchez l’une des extrémités, l’élastique se contracte rapidement et vous entendez un SNAP ! Le claquement est l’énergie potentielle libérée sous forme de son.
Parlons maintenant de la lumière. Le filament d’une ampoule à incandescence est constitué d’un matériau appelé tungstène. Le tungstène est constitué de molécules, c’est-à-dire d’un ensemble d’atomes reliés entre eux. L’atome possède un centre appelé noyau, autour duquel gravitent des électrons.
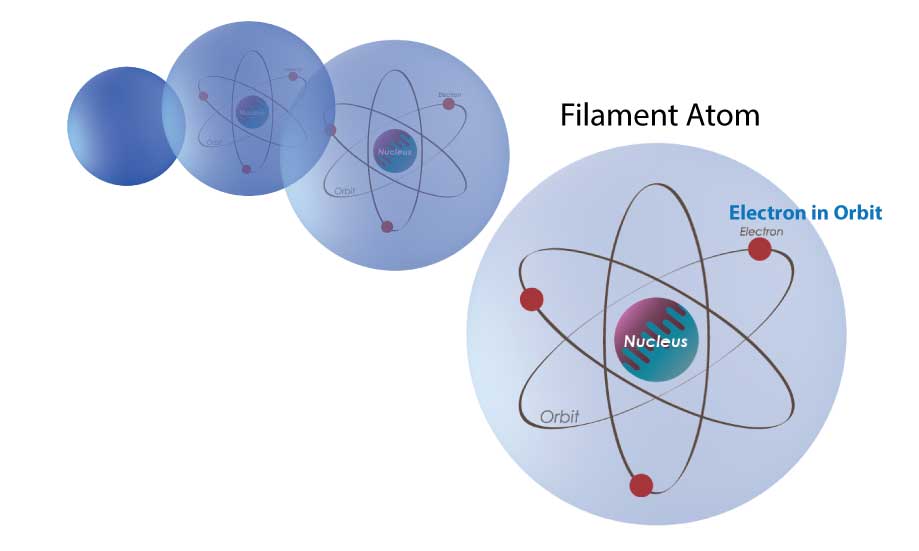
Fig 3a Filament d’une ampoule électrique
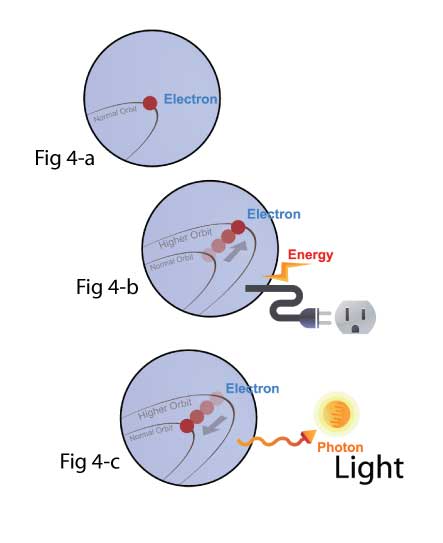
Commençons par l’électron sur son orbite basse naturelle (Fig 4-a).
Lorsque vous appliquez de l’énergie ou de l’électricité à l’ampoule, l’électron de l’atome du filament sera excité vers une orbite plus élevée et obtiendra de l’énergie potentielle (Fig. 4-b).
Lorsque l’électron revient à son état inférieur ou naturel (figure 4-c), il libère l’énergie – mais au lieu d’un son, il libère un photon de lumière.
Par conséquent, la lumière est simplement une libération d’énergie – et bien que d’autres types de lumières (LED, fluorescentes, etc.) diffèrent à bien des égards, elles ont toujours le même résultat final d’émettre des photons de lumière en permettant aux électrons de passer d’orbitales ou d’états supérieurs à des orbitales ou des états inférieurs.
Les électrons ne restent pas sur une orbite plus élevée, même avec une électricité constante.
Pourquoi les électrons ne continuent-ils pas à rester sur une orbite plus élevée – après tout, l’électricité est appliquée en permanence.
Les électrons en orbite haute sont comme une corde raide. Ils sont toujours dans un état très précaire, instable, et il est facile pour eux de tomber de leur orbite haute. Mais pourquoi les électrons sont-ils instables dans cet état ?
Physique et mécanique quantique
En bref, les particules subatomiques comme les électrons sont bizarres. Ils vivent dans le monde de l’infiniment petit, celui de la mécanique quantique. Cela signifie que les choses ne se comportent pas de la même manière que notre propre existence terrestre, c’est-à-dire le toucher, l’ouïe, la vue et l’odorat.
L’existence même d’un électron à un moment donné est incertaine, ce qui rend sa position sur la corde raide précaire. Ils tombent donc facilement et émettent un photon de lumière.
Grâce à l’électricité constante qui est appliquée, l’électron suivant est élevé à l’état supérieur, et il retombe bientôt – et c’est cette montée et descente continue de milliards d’électrons qui nous donne ce flux de lumière provenant d’une ampoule électrique.
Vue classique et quantique des électrons (approfondissement).
Certains diront que ma description classique de l’atome, du noyau et des électrons en orbite est inexacte. Je suis d’accord, mais c’est ainsi qu’on l’enseigne encore dans les salles de classe pour aider les élèves à se familiariser avec les complexités de la physique et de la chimie.
Dans le monde quantique, l’électron existe sous la forme d’un nuage d’électrons. Cela signifie que l’électron est toujours en train d’apparaître et de disparaître autour du noyau, mais qu’il n’est jamais au même endroit, à moins qu’on ne l’observe.
Ne vous inquiétez pas si vous ne comprenez pas – même nos scientifiques les plus brillants n’ont pas encore réussi à démêler complètement la mécanique quantique. Mais c’est pour cela que les électrons restent bizarres et que leur position dans le temps et l’espace sera toujours précaire.
La lumière est à la fois une particule et une onde
Il est facile de percevoir la lumière comme une particule en raison de son comportement : Elle rebondit sur les murs et les miroirs, comme le ferait une balle de tennis. Bien que nous ne puissions pas voir les particules de lumière, nous en déduisons qu’elles le sont en raison de leur comportement.
En même temps, la lumière est aussi une onde, non pas parce que nous pouvons voir la lumière comme des ondes aqueuses, mais en raison de son comportement. Une expérience célèbre, appelée expérience de la double fente, a consisté à envoyer de la lumière à travers deux fentes et le résultat a été étonnamment similaire à la façon dont les vagues d’eau passent à travers ces mêmes fentes. La lumière se comportant à la fois comme une particule et comme une onde, on a considéré qu’elle était à la fois l’une et l’autre.
Utilisation d’un spectromètre pour distinguer les particules des ondes
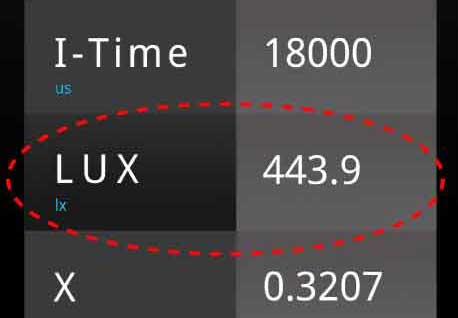
Un posemètre permet de mesurer et de voir les aspects particulaires et ondulatoires de la lumière. La lumière est constituée de particules appelées photons. Un spectromètre ou un luxmètre permet de mesurer le nombre de photons provenant de la lumière en mesurant le LUX ou le PPFD (lampes de culture). Plus le LUX est élevé, plus le nombre de photons frappant un mètre carré est important.
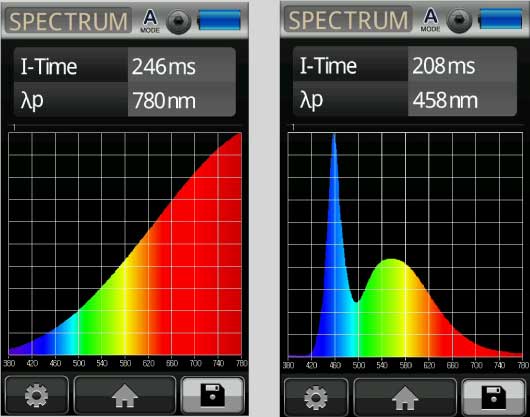
Un spectromètre est un appareil de mesure de la lumière sophistiqué qui peut également mesurer des ondes, et ces ondes ont une fréquence associée à une couleur spécifique. Les couleurs bleues ont des fréquences plus courtes et les couleurs rouges des fréquences plus longues.
Chaque photon a une longueur d’onde associée à une fréquence, qui détermine sa couleur, et un spectre pris par le spectromètre peut montrer le nombre relatif de photons pour chaque couleur visible dans une lumière.
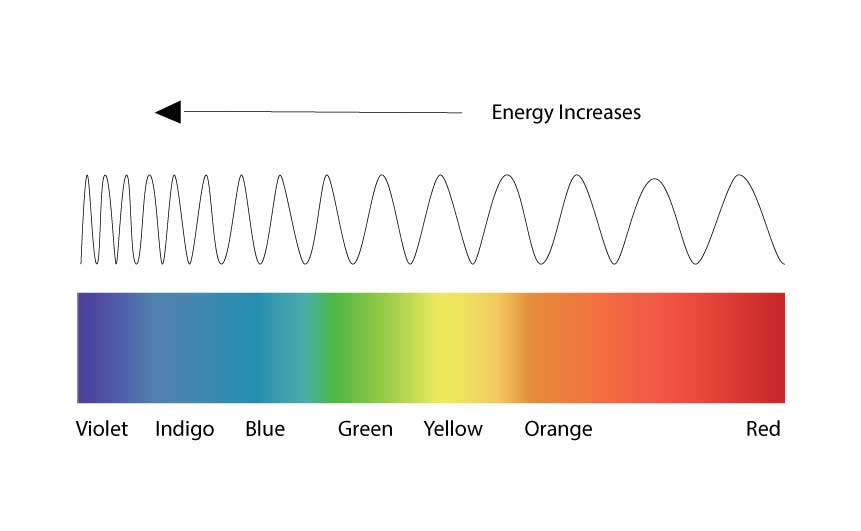
Fig 11 Les couleurs bleues ont des fréquences plus courtes, les rouges des fréquences plus longues.
Conclusion – Tirer les rideaux sur ce qu’est la lumière.
La lumière est une libération d’énergie, tout comme un élastique qui claque. Il faut comprendre que les électrons en orbite sont poussés vers un état supérieur. En raison des incertitudes liées à leur existence, les électrons retombent facilement dans leur état naturel, libérant de l’énergie sous forme de photons. Ce va-et-vient continu de milliards d’électrons produit un flux de lumière que nous n’avons plus besoin de prendre pour acquis.
Tout le monde peut être scientifique !

Fig. 12 Tous les éclairages utilisent des électrons en chute pour produire des photons de lumière.

Fig 13 – Spectromètre complet MK350S Premium
Le MK350S Premium est le spectromètre complet d’UPRtek.
Les projets critiques en matière de lumière sont confrontés à des instruments peu pratiques qui manquent de précision, de flexibilité, de commodité, de stockage de données et de connectivité avec d’autres appareils.
Le spectromètre portable MK350S Premium est un appareil polyvalent de qualité laboratoire utilisé par les chercheurs, les enseignants, les concepteurs d’éclairage, les fabricants de LED et les organismes de normalisation de l’éclairage. Il est doté d’une gamme complète de fonctions et de mesures d’éclairage permettant de relever tous les défis liés à l’éclairage sous le soleil.
Produit phare
Série de manuels

Le guide du scintillement
Tout ce que vous devez savoir sur Flicker, un artefact d'éclairage insidieux et potentiellement grave ayant un impact sur la sécurité visuelle des lieux publics comme les hôpitaux, les bureaux, les bibliothèques, etc.
A propos de l'UPRtek

United Power Research and Technology
UPRtek (est. 2010) est un fabricant d'instruments de mesure de la lumière portables et de haute précision ; spectromètres portatifs, appareils de mesure de la PAR, spectroradiomètres, solutions de calibrage de la lumière.
Le siège d'UPRtek, la R&D et la fabrication sont tous basés à Taiwan, avec une représentation mondiale par le biais de nos revendeurs certifiés.
Articles récents
Catégorie















0 commentaires